§9. Строение атома

Познакомить с ядерной моделью строения атома, нуклидами. Развить и укрепить представления о протонах, электронах и нейтронах, полученные в курсе физики.
Прямым доказательством сложности строения атома явилось и открытие самопроизвольного распада атомов некоторых элементов с испусканием невидимых глазу лучей. Это явление, открытое в 1896 г. французским ученым Анри Беккерелем, получило название радиоактивности.
В середине XIX в. атом считался элементарной, т. е. неделимой, частицей. Но уже к концу этого века появились неоспоримые доказательства сложности строения атома.
В 1897 г. английский физик Дж. Дж. Томсон установил существование в атоме электронов — отрицательно заряженных частиц.
Английский ученый Эрнест Резерфорд в 1911г. предложил схему строения атома, получившую название ядерной (планетарной) модели атома.
 Согласно этой модели, атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. Почти вся масса атома (более 99,96 %) сосредоточена в его ядре, диаметр которого приблизительно в 100 000 раз меньше диаметра всего атома.
Согласно этой модели, атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. Почти вся масса атома (более 99,96 %) сосредоточена в его ядре, диаметр которого приблизительно в 100 000 раз меньше диаметра всего атома.
Ядро атома также имеет сложное строение. Оно состоит из частиц двух типов: протонов и нейтронов.
В таблице приводятся основные характеристики частиц, входящих в состав атома:

Физический смысл атомного номера:
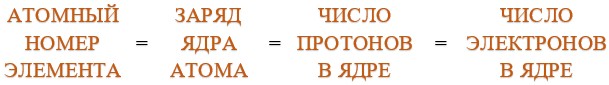
Например, атомный номер водорода H равен 1. Следовательно, заряд ядра его атома равен 1+ (т. е. ядро содержит только один протон), а вокруг ядра вращается один электрон с зарядом 1-.
Атомный номер следующего элемента гелия Не равен 2. Это означает, что заряд ядра его атома равен 2+, а общее число электронов в атоме также равно двум.
Увеличение атомного номера элемента связано с возрастанием числа протонов в ядре, т. е. с увеличением положительного заряда ядра.
Свойства атомов химических элементов, а также состав и свойства образуемых ими веществ находятся в периодической зависимости от зарядов атомных ядер.
Итак, сегодня мы узнали:
Атом — сложная электронейтральная частица, состоящая из положительно заряженного ядра и электронов.
Вся масса атома сосредоточена в его ядре, размеры которого примерно в 100 000 раз меньше размера всего атома.
Заряд ядра атома является главной характеристикой химического элемента, определяя все основные свойства атомов этого элемента.
Атомный номер химического элемента равен заряду ядра его атома, числу протонов в ядре и числу электронов в этом атоме.
Теги материала:



