урок 25. Понятие о кислотах

Кислоты – сложные вещества, содержащие водорода, способные замещаться на атомы металла, и кислотные остатки.
По наличию атомов кислорода неорганические кислоты делятся на кислородсодержащие (H2S04, Н3РО4, HNO3 и другие) и бескислородные (НСI, H2S и другие).
По количеству атомов водорода кислоты делятся на одноосновные (HCI), двухосновные (H2S) и трехосновные (Н3Р04).
Названия кислот состоят из двух слов — прилагательного, производного от корня кислотообразующего элемента (S, Р, N и т. д.), и слова «кислота»: серная кислота, азотная кислота, фосфорная кислота.
В случае бескислородных кислот к корню от названия кислотообразующего элемента добавляют окончание «водородная»: H2S — сероводородная кислота, HCI — хлороводородная кислота.
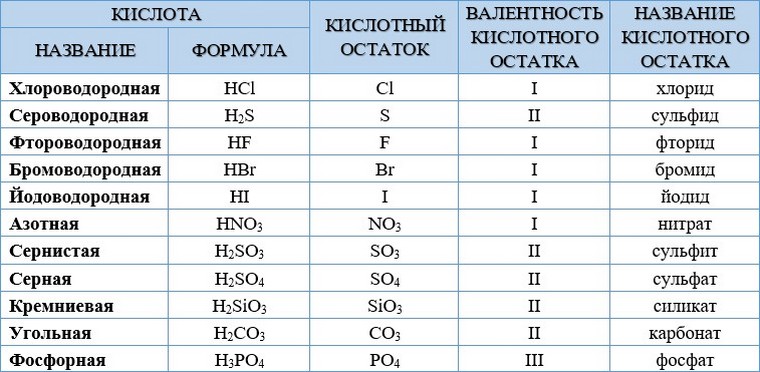
НАЗВАНИЯ КИСЛОТ
ФИЗИЧЕСКИЕ СВОЙСТВА КИСЛОТ
- Агрегатное состояние: при обычных условиях кислоты существуют в жидком и твердом агрегатных состояниях. Так, фосфорная кислота Н3РО4, при комнатной температуре — твердое вещество. При этих же условиях серная кислота H2SO4 — что не имеющая запаха вязкая жидкость. Она почти в 2 раза тяжелее воды. Хлороводородная кислота НCI — раствор газа хлороводорода в воде. Раствор этой кислоты имеет характерный запах;
- В большинстве случаев кислоты растворяются в воде. Исключение — кремниевая кислота H2SiO3;
- Кислоты изменяют окраску некоторых органических веществ;
- Имеют кислый вкус (пробовать кислоты на вкус, как и любые другие вещества, запрещается — можно получить ожог полости рта!);
- Оказывают разъедающее действие на кожу человека, ткани, бумагу, древесину и другие материалы.
Индикаторы — органические вещества, изменяющие свою окраску в присутствии кислот и некоторых других веществ.

Теги материала:



