урок 14. Закон сохранения массы веществ

На основе работ М. В. Ломоносова и А. Лавуазье был сформулирован закон сохранения массы веществ.
Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ.
При химических реакциях атомы не исчезают бесследно и не возникают из ничего. Их число остается неизменным. Атак как они имеют постоянную массу, то и масса образованных ими веществ также остается постоянной.
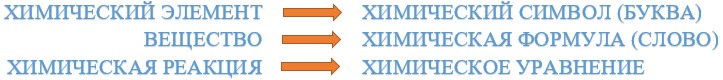
Химические элементы обозначают химическими символами, состав веществ записывается при помощи химических формул, химические реакции выражают при помощи химических уравнений, т. е. так же, как из букв составляются слова, из слов — предложения:
Уравнение химической реакции (химическое уравнение) — это условная запись реакции при помощи химических формул и специальных знаков.

Специальными знаками, которые используются при написании химических реакций, являются:
- «+» (плюс), соединяющий формулы веществ в каждой части уравнения,
- «=» (равно), который связывает левую и правую части уравнения,
- коэффициенты - числа перед формулами веществ, показывают число молекул или формульных единиц.
- знак «↓», если вещество образует осадок, например:
$\mathrm{AgNO_{3}+HCl=AgCl \downarrow + HNO_{3},}$
- знак «↑», если в результате реакции образуется газ, например:
$\mathrm{C+O_{2}=CO_{2} \uparrow}$
- «+Q» - выделение тепла,
- «-Q» - поглощение тепла.
Часто в уравнениях реакций над знаком «=» указывают условия их протекания: нагревание (t), облучение светом (hv) и другие.
Теги материала:



