урок 14. Уравнения химических реакций
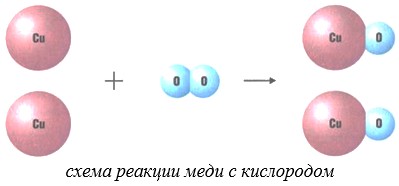
Составлять химические уравнения и производить расчеты по ним нужно, опираясь на закон сохранения массы веществ при химических реакциях. Рассмотрим, как можно составить химическое уравнение, на примере реакции меди с кислородом.
- Слева запишем исходные вещества, справа — продукты реакции. Если веществ два и более, соединяем их знаком «+». Между левой и правой частями пока поставим стрелку.
Подобное выражение называют схемой химической реакции. Запишем эту схему при помощи химических формул:
$\mathrm{Cu+O_{2} \rightarrow CuO}$
- Число атомов кислорода в левой части схемы равно двум, а в правой — одному. Число атомов каждого элемента до реакции должно быть равно числу атомов этих же элементов после реакции. Чтобы уравнять число атомов кислорода в левой и правой частях схемы, перед формулой СuО поставим коэффициент 2:
$\mathrm{Cu + O_{2} \rightarrow 2CuO}$
- Теперь число атомов меди после реакции (в правой части) равно двум, а до реакции (в левой части) только одному, поэтому перед формулой меди Сu поставим коэффициент 2.
$\mathrm{2Cu+O_{2} \rightarrow 2CuO}$
- В результате произведенных действий число атомов каждого вида в левой и правой частях одинаково, что дает нам основание заменить стрелку на знак «=» (равно). Схема превратилась в уравнение химической реакции.
Обратите внимание: если для протекания реакции требуется повышенная температура, то над знаком равенства нужно поставить значок t (данная реакция протекает при температуре t = 400 - 500 °C).
$\mathrm{2Cu+O_{2} \overset{t}{=} 2CuO}$
Это уравнение читается так: два купрум плюс о-два равно два купрум-о.
Теги материала:



